
Του Prof. Dr. Stephan Sander-Faes
Οι δύο ισχυροί όροι που χρησιμοποιούνται εδώ – “απάτη” και “ανικανότητα” αντίστοιχα – απαιτούν εξίσου ισχυρά αποδεικτικά στοιχεία. Σε αυτό το άρθρο, λοιπόν, εξετάζουμε προσεκτικά δύο (οιονεί) επίσημα έγγραφα συγκεκριμένα: από τη μία πλευρά, το δίπλωμα ευρεσιτεχνίας αριθ. 10,485,884 B2 των ΗΠΑ της 26ης Νοεμβρίου 2019 των Sahin et al. (ναι, αυτός είναι ο ιδρυτής της BioNTech) και, από την άλλη πλευρά, τα έγγραφα έγκρισης του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMA) της 19ης Φεβρουαρίου 2021 σχετικά με τη δραστική ουσία της BioNTech/Pfizer, η οποία κυκλοφορεί με την εμπορική ονομασία “Comirnaty”. Η σύγκριση αυτών των εγγράφων υποδεικνύει άκρως αμφίβολες δραστηριότητες των κατασκευαστών και των ρυθμιστικών αρχών φαρμάκων, για να μην αναφέρουμε “τους εμπειρογνώμονες”, “τους πολιτικούς” και τα “κορυφαία και ποιοτικά μέσα ενημέρωσης”.
Πρώτα απ’ όλα: τα αποσπάσματα που παρατίθενται παρακάτω προέρχονται από αυτά τα δύο έγγραφα, τα οποία είναι αναρτημένα εδώ και μπορούν να τα δουν οι πολίτες, και από τα οποία προέρχονται και τα στιγμιότυπα οθόνης που έχουν ενσωματωθεί εδώ:
US Patent No. 10,485,884 B2, 26 Nov. 2019, ιδιοκτησίας Sahin et al (πηγή).
EMA, έγγραφο με αριθμό EMEA/H/C/005735/0000, 19 Φεβ. 2021 (πηγή).Δίπλωμα ευρεσιτεχνίας ΗΠΑ αριθ. 10,485,884 B2, 26 Νοεμ. 2019, κάτοχος: Sahin et al.
Αυτό που προκαλεί εντύπωση σε αυτό το έγγραφο είναι πρώτα απ’ όλα η ημερομηνία, διότι τα εν λόγω δικαιώματα ευρεσιτεχνίας όχι μόνο καταχωρίστηκαν ή δημοσιεύθηκαν από το Γραφείο Διπλωμάτων Ευρεσιτεχνίας των ΗΠΑ αρκετούς μήνες πριν από την κήρυξη της λεγόμενης “πανδημίας” από τον ΠΟΥ. Αντιθέτως, από την τεκμηρίωση προκύπτει ότι η κατάθεση (αριθ. 14/388,192) φέρει ημερομηνία 25 Μαρτίου 2013, γεγονός που καθιστά τουλάχιστον αμφισβητήσιμη την επανειλημμένα επαναλαμβανόμενη αναφορά ότι οι ουσίες modRNA αναπτύχθηκαν “σε χρόνο ρεκόρ”. Παρεμπιπτόντως πρέπει να αναφερθεί ότι οι αιτούντες αναφέρονται ρητά σε μια “διεθνή αίτηση” (αρ. PCT/EP2012/001319) με ημερομηνία 26 Μαρτίου 2012 (!).
Τις πολύ πιο σημαντικές λεπτομέρειες, ωστόσο, πρέπει να τις δούμε με ηρεμία. Το δίπλωμα ευρεσιτεχνίας ΗΠΑ αριθ. 10,485,884 B2 αφορά την “ανοσοθεραπεία, ιδίως τη θεραπεία του καρκίνου” (παρ. 1. Σημειώστε ότι το έγγραφο δεν έχει σελιδοποίηση και ότι τα αποσπάσματα που παρατίθενται παρακάτω αρχίζουν από τη σελίδα 43 του 69σέλιδου εγγράφου PDF- πριν από αυτό υπάρχει ένας αριθμός γραφικών, απεικονίσεων κλπ).

Στις ίδιες σελίδες, λίγο πιο κάτω στο κείμενο, υπάρχουν συνολικά τρεις σχετικές αναφορές:
–Το δίπλωμα ευρεσιτεχνίας περιγράφει τη
στοχευμένη εφαρμογή αυτής της θεραπείας στους λεμφαδένες, η οποία,
ωστόσο, περιγράφεται ως “πολύ περίπλοκη” λόγω της απαιτούμενης ιατρικής
εμπειρίας- οι εναλλακτικές λύσεις περιλαμβάνουν την ενδοφλέβια ή
ενδοδερμική (δηλαδή με ένεση) χορήγηση ή την εισπνοή των δραστικών
ουσιών.
–Τα λεγόμενα “λιποπλέγματα” (λιπιδικά νανοσωματίδια) που
χρησιμοποιούνται για το σκοπό αυτό αποτελούνται από δύο κύρια μέρη, τα
θετικά φορτισμένα λίπη (“λιποσώματα”) και τα αρνητικά φορτισμένα μέρη
modRNA ή DNA.
–Η ηλεκτρική φόρτιση είναι απαραίτητη για την αποτελεσματική μεταφορά
(διαμόλυνση) της πληροφορίας modRNA ή DNA στο κύτταρο (ή στα
κύτταρα-στόχους).
Ποια είναι όμως τα προβαλλόμενα προβλήματα μιας τέτοιας προσέγγισης;
Οι περισσότερες φυσικές μεμβράνες είναι αρνητικά φορτισμένες και επομένως η ηλεκτροστατική αλληλεπίδραση μεταξύ των θετικά φορτισμένων “λιποπλεξών” και της αρνητικά φορτισμένης κυτταρικής μεμβράνης μπορεί να διαδραματίσει ρόλο στην πρόσληψη αυτών των “λιποπλεξών” στο κύτταρο.
Τι μπορεί να πάει στραβά στη διαδικασία;

Δυστυχώς, έχει διαπιστωθεί αυξημένη τοξικότητα για τα θετικά φορτισμένα λιποσώματα και τα λιποπλέγματα, γεγονός που μπορεί να αποτελέσει πρόβλημα για τη χρήση τέτοιων σκευασμάτων ως φαρμάκων.
Αυτό είναι ένα θεμελιώδες πρόβλημα – κίνδυνος – επειδή οι παράγοντες mod-RNA της BioNTech/Pfizer και της Moderna χρησιμοποιούν την ίδια τεχνολογία που περιγράφεται εδώ για τις ενέσεις Covid. Για να μπορέσουμε να ταξινομήσουμε τις απορρέουσες ανησυχίες με μεγαλύτερη ακρίβεια, πρέπει να εξετάσουμε για λίγο τις συγκεκριμένες ηλεκτροστατικές ιδιότητες αυτών των “Liploplexes”.
ρυθμιστικό pH, νανοσωματίδια modRNA και οι σχετικοί κίνδυνοι.
Τούτο είναι αναπόφευκτο, καθώς το κείμενο της πατέντας της BioNTech αναφέρει λίγο πιο κάτω τα εξής:

Διαπιστώνουμε ότι: οι ρυθμιστές pH είναι απαραίτητοι, οδηγούν ενδεχομένως σε “συσσωμάτωση των λιποπλεξών” και είναι συνεπώς “ακατάλληλοι” για “παρεντερική χρήση” – δηλαδή για ενδοδερμική χορήγηση με ένεση ή “εμβολιασμό”.

Επιπλέον, η χρήση “χλωριούχου νατρίου” (vulgo: αλατούχο διάλυμα) είναι ακατάλληλη επειδή οδηγεί σε “σημαντικά αυξημένο/συσσωρευμένο μέγεθος σωματιδίων”. Κατά συνέπεια, “ένα θετικό φορτίο είναι ακατάλληλο για τη σταθεροποίηση των λιποπλεξών” και “η συσσώρευση είναι αναμενόμενη”.
Θεωρούμε λοιπόν ότι οι “σωστές” ηλεκτροστατικές ιδιότητες είναι απαραίτητες για να εξασφαλιστεί η προβλεπόμενη λειτουργία των παραγόντων modRNA. Παρεμπιπτόντως, όπως σημειώνουν οι Sahin et al. στην αίτηση για δίπλωμα ευρεσιτεχνίας, είναι αυτές οι βιοχημικές πτυχές που συμβάλλουν στην αστάθεια των λιποπλεξών (“λιπιδικά νανοσωματίδια”), με συνέπεια να γίνεται αναφορά για συσσωμάτωση.
Οι ρυθμιστικοί διαλύτες pH, όπως ο ρυθμιστικός φυσιολογικός ορός με φωσφορικά άλατα (PBS για συντομία, από το phosphate-buffered saline), είναι τα λεγόμενα ισοτονικά αλατούχα διαλύματα που χρησιμοποιούνται ευρέως στη βιοχημική έρευνα λόγω της σταθερής τιμής του pH τους (7,4).
Ωστόσο, σύμφωνα με τα έγγραφα διπλωμάτων ευρεσιτεχνίας της BioNTech, αυτά έχουν δυνητικά σοβαρές επιπτώσεις στον άνθρωπο όσον αφορά την τοξικότητά τους, καθώς έχει αποδειχθεί ότι οδηγούν στο σχηματισμό θρόμβων:

Τα γεγονότα αυτά ήταν γνωστά κατά τη στιγμή της “άδειας κυκλοφορίας υπό όρους” από τον ΕΜΑ.
Τι γνώριζε ο ΕΜΑ το χειμώνα του 2020/21;
Εν ολίγοις: όχι πάρα πολλά, όπως δείχνει αυτό το απόσπασμα στη σελ. 140 (“MAH” = “κάτοχος άδειας κυκλοφορίας”, δηλαδή ο κατασκευαστής με άδεια κυκλοφορίας υπό όρους”):

Τα δύο συστατικά ALC-0315 και ALC-0159, όπως προκύπτει από μια ματιά στη σελίδα 23 του ίδιου εγγράφου – σε αντίθεση με τα άλλα συστατικά του φαρμακευτικού προϊόντος Comirnaty – ταξινομούνται ως “νέα έκδοχα”, δεδομένου ότι “δεν έχουν χρησιμοποιηθεί ποτέ πριν σε φαρμακευτικό προϊόν στην Ευρώπη” και “δεν είναι καταχωρισμένα στη Φαρμακοποιία της ΕΕ” (το ηλεκτρονικό μητρώο όλων των φαρμακευτικών προϊόντων ή συστατικών).
Επιπλέον, τα εν λόγω συστατικά ALC-0315 και ALC-0159 δεν είναι καταχωρημένα στο μητρώο C&L του Ευρωπαϊκού Οργανισμού Χημικών Προϊόντων (ECHA), παρόλο που ο ίδιος αυτός ο οργανισμός έχει την εντολή να καταχωρίζει όλες τις χημικές ουσίες που χρησιμοποιούνται στην ΕΕ/ΕΟΧ.
Και αυτό παρά το γεγονός ότι η ίδια η ΕΕ (πηγή) αναφέρει ότι “οι μη καταχωρημένες χημικές ουσίες δεν μπορούν να διατίθενται στην αγορά”.
Το “έγγραφο αδειοδότησης” του ΕΜΑ που παραπέμπει στην αρχή αυτού του άρθρου αναφέρει επίσης:
Δεν έχουν παρουσιαστεί μελέτες σχετικά με τη γονοτοξικότητα ή την καρκινογένεση. Τα συστατικά του εμβολίου είναι λιπίδια και RNA, τα οποία δεν αναμένεται να έχουν γονιδιοτοξικό δυναμικό (σελ. 55)….
Δεν έχουν παρουσιαστεί μελέτες σχετικά με τη γονοτοξικότητα ή την καρκινογένεση. Τα συστατικά του εμβολίου (λιπίδια και mRNA) δεν αναμένεται να έχουν γονοτοξικό δυναμικό. Αυτό είναι αποδεκτό από την CHMP [Επιτροπή Φαρμακευτικών Προϊόντων για τον άνθρωπο] (σ. 56).
Αυτό και η “άδεια κυκλοφορίας υπό όρους” έρχονται σε αντίθεση με τον κανονισμό ΕΕ 2018/1881, ο οποίος, μεταξύ άλλων, προσδιορίζει τους κανόνες σχετικά με τα νανοϋλικά ως εξής (308/6):
Η αξιολόγηση θα πρέπει πάντοτε να περιλαμβάνει δήλωση σχετικά με το αν η ουσία ή, κατά περίπτωση, οι νανομορφές της πληρούν τα κριτήρια του κανονισμού (ΕΚ) αριθ. 1272/2008 για την ταξινόμηση ως καρκινογόνου κατηγορίας 1Α ή 1Β, μεταλλαξιογόνου για τα γεννητικά κύτταρα κατηγορίας 1Α ή 1Β ή τοξικής για την αναπαραγωγή κατηγορίας 1Α ή 1Β.
Ωστόσο, από τις 7 Δεκεμβρίου 2021, αυτό εξακολουθούσε να εμφανίζεται ως “δεν υπάρχουν διαθέσιμες πληροφορίες” στη σχετική τεκμηρίωση της Pfizer:
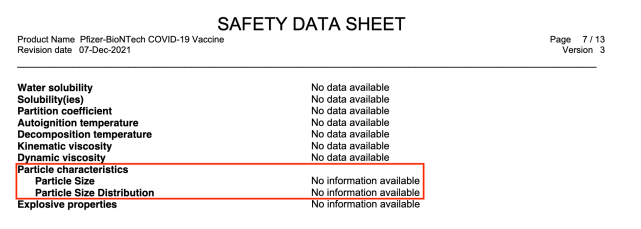
Το ίδιο ισχύει και για τις τοξικολογικές μελέτες, οι οποίες επίσης δεν είχαν διεξαχθεί έως τον Δεκέμβριο του 2021:

Ανικανότητα ή διαφθορά;
Όλα αυτά αποδεικνύουν τεράστια προβλήματα με την αρχική “άδεια κυκλοφορίας υπό όρους”, δεδομένου ότι τα προβλήματα – τα οποία παρεμπιπτόντως αφορούσαν και τη δραστική ουσία modRNA της Moderna εκτός από το προϊόν της BioNTech/Pfizer – ήταν γνωστά από τα έγγραφα των διπλωμάτων ευρεσιτεχνίας “πριν από την Covid”.
Σε κάθε περίπτωση, αυτό εγείρει το βασικό ερώτημα: τι γνώριζαν οι αρχές έγκρισης και εποπτείας (sic) για τα έγγραφα αυτά και πότε;
Οι συνέπειες της χρήσης διαλυμάτων αλάτων ρυθμισμένων με φωσφορικά άλατα για το “τέντωμα” των δραστικών ουσιών οδηγούν σε ερωτήματα σχετικά με την επάρκεια των “εμπειρογνωμόνων” στις αρχές χορήγησης αδειών και εποπτείας, απλώς και μόνο λόγω των ηλεκτροστατικών ιδιοτήτων των λιπιδικών νανοϋλικών- επειδή ο ρόλος των θετικών ή αρνητικών φορτίων των νανοϋλικών δεν έχει πρωτίστως καμία σχέση με τα “νέα” συστατικά των δραστικών ουσιών modRNA.
Επομένως, προκύπτει και εδώ το ερώτημα για την ποιότητα όχι μόνο των δραστικών ουσιών κατά της covid, αλλά και των άλλων προϊόντων που “ελέγχονται” από τις αδειοδοτούσες και εποπτεύουσες αρχές, τα οποία χρησιμοποιούνται καθημερινά στα φαρμακεία, στα ιατρεία και στα νοσοκομεία χωρίς περαιτέρω…έγνοιες.
Η ηχηρή….σιωπή των ρυθμιστικών αρχών
Λόγω της σιωπηρής αντικατάστασης μόνο των ρυθμισμένων με φωσφορικά άλατα διαλυμάτων στα προϊόντα modRNA της BioNTech/Pfizer και της Moderna από το φθινόπωρο του 2021, υπάρχουν τουλάχιστον ενδείξεις ότι οι φαρμακευτικοί κολοσσοί απομακρύνονται από τα ηλεκτροστατικά προβλήματα που ήταν γνωστά στη προ-Covid εποχή.
Η μεγάλη “καινοτομία” ήταν ότι η κατάψυξη των προϊόντων modRNA, η οποία προηγουμένως προκαλούσε προβλήματα, δεν είναι πλέον απαραίτητη. (Αυτό ήταν απαραίτητο για τον ίδιο ακριβώς λόγο ότι τα νανοσωματίδια διαφορετικά δεν θα παρέμεναν στατιστικά σταθερά ή δεν θα είχαν επαρκή ακεραιότητα).
Όπως ανέφερε ο EMA στον ιστότοπό του σε δελτίο τύπου (18 Οκτωβρίου 2021), το πλέον “έτοιμο προς χρήση σκεύασμα του Comirnaty δεν χρειάζεται να αραιωθεί πριν από τη χορήγηση” και μπορεί “να αποθηκευτεί σε θερμοκρασία 2-8 °C για διάστημα έως και ενός μήνα”. Επισημάνθηκαν σαφώς οι βελτιώσεις για “την αποθήκευση, τη μεταφορά και τις υλικοτεχνικές επιλογές για τη διανομή και τη χορήγηση του εμβολίου”, αλλά όχι ο ρόλος που παίζουν τα ρυθμισμένα με φωσφορικά άλατα διαλύματα (ηλεκτρολύτες) στη σταθερότητα ή την ακεραιότητα των δραστικών συστατικών.
Η καταχώριση του τροποποιημένου δραστικού συστατικού “Comirnaty Tris/Sucrose” δείχνει ότι η σύνθεση είναι σχεδόν πανομοιότυπη με το προϊόν που εγκρίθηκε υπό όρους στα τέλη του 2020 – εκτός από τα ρυθμισμένα με φωσφορικά άλατα διαλύματα (ηλεκτρολύτες). Παρεμπιπτόντως, αυτό ισχύει και για τη δραστική ουσία modRNA της Moderna, όπως προκύπτει από την τεκμηρίωση που υποβλήθηκε στον EMA με ημερομηνία 11 Μαρτίου 2021 (σελ. 26):

Τόσο η BioNTech/Pfizer όσο και η Moderna έχουν αφήσει αμετάβλητα τα “υπόλοιπα” δραστικά συστατικά, όμως από το φθινόπωρο του 2021 χρησιμοποιούν τους ίδιους ρυθμιστές (tromethamol και tromethamol CHI, αντίστοιχα).
Ο Dr. Gabriele Segalla, πρόεδρος του διοικητικού συμβουλίου και “επικεφαλής επιστήμονας” της Multichem R&D, εταιρείας με έδρα την Ιταλία, συνοψίζει αυτές τις αθέατες αλλαγές στην εργασία “Chemical-Physical Criticality and Toxicological Potential of Lipid Nanomaterials Contained in a COVID-19mRNA Vaccine“, International Journal of Vaccine Theory, Practice, and Research, 3 (1) (2023): 787-817, ως εξής (σελ. 808-12- πηγή):
Αυτή η διαδικασία αποκλεισμού του ηλεκτρολύτη μπορεί να φαίνεται συνηθισμένη στον απλό άνθρωπο, αλλά στην πραγματικότητα είναι αποκαλυπτική για τους ειδικούς στον τομέα των κολλοειδών συστημάτων…
Από τεχνική άποψη, στο νέο έτοιμο προς χρήση σκεύασμα, το προηγούμενο ρυθμιστικό pH PBS (ηλεκτρολυτικό, ανόργανο) έχει εξαλειφθεί και αντικατασταθεί από ένα άλλο πολύ κοινό ρυθμιστικό, το λεγόμενο ρυθμιστικό Tris, το οποίο χρησιμοποιείται ευρέως στη βιολογία για την παρασκευή διαλυμάτων με ελεγχόμενο pH (ιδίως για νουκλεϊκά οξέα)…
Σε ποιο βαθμό έχει βελτιωθεί το προφίλ σταθερότητας σε σχέση με την προηγούμενη έκδοση δεν αποκαλύπτεται δυστυχώς…
Δυστυχώς, οι απαντήσεις σε αυτά τα ερωτήματα μάλλον δεν θα δοθούν ποτέ, καθώς πιθανότατα θα χαρακτηριστούν ως εμπιστευτικές επιχειρηματικές πληροφορίες και συνεπώς θα υπόκεινται σε απόκρυψη. Παρ’ όλα αυτά, το λογικό συμπέρασμα παραμένει ότι το εμβόλιο PBS/σακχαρόζη Comirnaty (το οποίο εγχέεται σε δισεκατομμύρια δόσεις) έπρεπε να αλλάξει όχι μόνο για να γίνει ευκολότερο στη χρήση, αλλά κυρίως για να βελτιωθεί η σταθερότητά του, αναπόφευκτα…
Στη σελ. 814, ο Segalla επισημαίνει με τη σειρά του τις συνέπειες αυτής της προσέγγισης:
Όλες οι συστάσεις που αναφέρονται στην προαναφερθείσα πατέντα της BioNTech του 2019 έχουν ξεδιάντροπα διαψευστεί ή αγνοηθεί τόσο από την Pfizer-BioNTech όσο και από τους φορείς πιστοποίησης από το 2020, τόσο όσον αφορά τον τύπο του σκευάσματος Comirnaty (ιοντικό/ηλεκτρολυτικό) όσο και την προβλεπόμενη χρήση του (ενδομυϊκή ένεση).
Τέλος, το φάρμακο Comirnaty/PBS Sucrose της Pfizer-BioNTech, το οποίο εγκρίθηκε από τον EMA το 2020, παρουσιάζει σοβαρά και προφανή χημικο-φυσικά και τοξικολογικά προβλήματα που έρχονται σε ανοιχτή αντίθεση με τις συγκεκριμένες και σχετικές συστάσεις που η ίδια η BioNTech ισχυρίζεται στην προαναφερθείσα πατέντα της.
Φυσικά, η “πανδημία” που κήρυξε ο ΠΟΥ είναι ένα πολύπλευρο φαινόμενο, αλλά σε κάθε περίπτωση θα αναγκαστούν να βρεθούν σύντομα ενώπιον των δικαστηρίων τα στελέχη και τα μέλη του διοικητικού συμβουλίου της BioNTech/Pfizer , της Moderna κλπ ή των παραγόντων των ρυθμιστικών και αδειοδοτικών αρχών.
Η συνεχιζόμενη έγκριση, προώθηση και χορήγηση αυτών των προϊόντων modRNA είναι κάτι περισσότερο από – ένα αποδεδειγμένο ποινικό αδίκημα, που διαπράττεται καθημερινά παρά την καλύτερη κρίση τους.
Όσοι στις εποπτικές και ρυθμιστικές αρχές ή μεταξύ των “ειδικών”, των πολιτικών και των “δημοσιογράφων”, μπροστά σε αυτά τα έγγραφα, συνεχίζουν να επιδεικνύουν άγνοια απλώς επιδεικνύουν τη δική τους ανικανότητα, η οποία, όπως γνωρίζουμε, δεν προστατεύει από την επιβολή αυστηρών ποινών.
Ημερομηνία δημοσίευσης: 06.10.2023
eyewideopen.org